植入式传感器的电极通常由生物相容性材料制成,但作为异物,难以完全避免生物污染和异物反应。由于宿主将多数植入传感器视为“异物”,在伤口愈合过程中触发复杂的级联免疫信号:纤维蛋白原和其他蛋白质与植入物表面结合,然后吸引巨噬细胞迁移到局部,释放炎性细胞因子,从而刺激静止的成纤维细胞转化成肌成纤维细胞以合成前胶原蛋白。前胶原蛋白交联成熟后与其他细胞外基质蛋白形成一个致密的纤维囊,包裹住植入的“异物”,阻碍物质扩散,严重影响了生物传感器和药物/细胞递送装置等器件发挥正常功能。
例如,动态血糖监测仪因纤维化包裹和生物污染导致的噪声,需要进行每日校准,使用期限仅7~14天。减轻或消除异物反应不仅可以提高传感器的检测性能,也能延长其使用寿命,更能有效避免局部炎症和纤维化反应。因此,电极外部最好涂覆有用于防止传感器结垢的生物相容性层。例如,内源性气体小分子一氧化氮(NO)能抑制血小板黏附和活化、炎症反应和细菌生长,因此,在器件表面修饰释放NO的聚合物涂层可以有效改善传感器的生物相容性。
除了生物污染对检测性能的不利影响,分析物本身的电氧化产物在电极表面富集也是电极结垢和传感器信号衰减的原因之一。5-HT是一种具有良好电活性的兴奋性神经递质,可以在碳电极表面直接氧化形成电流,但随着氧化反应的发生,产物迅速电聚合,低聚物通过π-π堆积作用强烈吸附在电极表面,这种结垢效应大大降低了电流响应和灵敏度,使电流型传感器失效。
因此,Zhu等提出了一种无氧化还原反应的电位传感平台(GRP),用于活体动物脑内5-HT的自驱动传感。该GRP系统包括对5-HT敏感的阳极指示电极和嵌入K₂IrCl₆溶液中的阴极参比电极,只有当指示电极上发生分子识别,在双极体系中形成具有净负Gibbs自由能的电路时,传感器才能在静态条件下产生浓度依赖性开路电位响应。
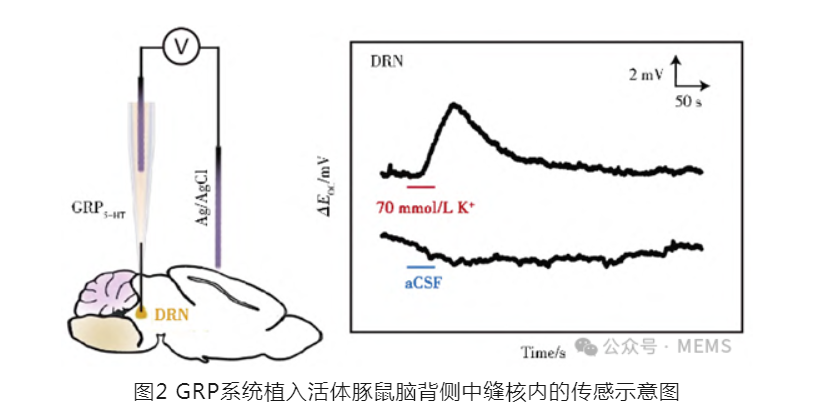
关键点在于,GRP系统工作环境接近零电流,因此在测量期间造成的氧化反应最弱,有效减少了常规安培传感器在5-HT检测时容易出现的电极钝化。此外,由于电势输出和分析物浓度符合能斯特方程,GRP传感器的灵敏度与电化学表面积无关,进一步消除了生物环境内丰富的蛋白质对电极的潜在生物污染效应。如图2所示,植入豚鼠的背侧中缝核(DRN)后,该GRP系统能在50 s内准确检测到高K⁺刺激(70 mmol/L)诱导的5-HT内源性释放,充分证明了植入式传感器在活体内优异的时空分辨率。
前,部分植入式电化学生物传感器已经进入商业化时代。例如,Senseonics公司生产的Eversense E3皮下植入式动态血糖仪于2022年获美国FDA批准上市。与多数连续血糖监测仪的构造相同,Eversense E3由传感器和发射器组成,通过蓝牙将血糖信息传输到移动设备中,能够提供长达180天的动态血糖值;Neuralink公司发明的植入式脑机接口设备通过在大脑中植入电极丝来“读取”脑电波信号,有望“解码大脑”以解决阿尔茨海默病、脑卒中、癫痫等脑部疾病。总之,作为组织与电子的接口,植入式传感器在生物电子医疗领域发挥着重要作用。